Chem:新材料的开发有助于苯的捕获和分离!
苯是一种重要的挥发性有机化合物(VOC),具有高毒性,对人类健康构成严重威胁的化合物。在石化工业中,苯和环己烷的分离对于高纯度环己烷的生产至关重要。传统的吸附剂如活性炭和沸石常常受到结构紊乱的限...
苯是一种重要的挥发性有机化合物(VOC),具有高毒性,对人类健康构成严重威胁的化合物。在石化工业中,苯和环己烷的分离对于高纯度环己烷的生产至关重要。传统的吸附剂如活性炭和沸石常常受到结构紊乱的限制,难以观察到结合位点和主客体之间的相互作用。然而,苯不仅是一种重要的空气污染物,也是合成环己烷所必需的关键化学原料。由于苯和环己烷的沸点仅相差0.6°C,它们之间的分离极具挑战性。
鉴于此,近期由新入职北京大学化学与分子工程学院的杨四海教授和曼彻斯特大学课题组在Chem上发表了题为“Control of the pore chemistry in metal-organic frameworks for efficient adsorption of benzene and separation of benzene/cyclohexane”的研究成果。
概述
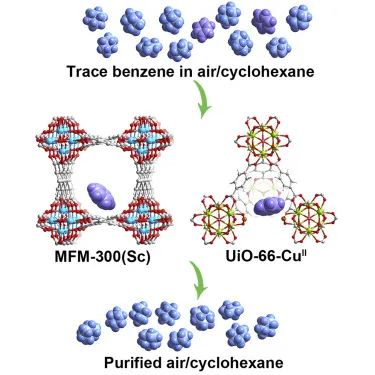
该研究主要报道了两类坚固型MOF(金属-有机框架)材料(MFM-300和UiO-66)的孔道化学精确调控设计,以实现苯在低压下的高吸附性能,并在液相条件下高效分离苯/环己烷,即使存在水也可以实现分离。通过将原子分散的Cu(Ⅱ)位点装饰在UiO-66缺陷结构缺陷(丢失连接体)中,结果得到了UiO-66-CuⅡ材料,在1.2 mbar和298 K下对苯具有杰出且可逆的吸附性能,吸附量达到3.92 mmol g-1,展示了其捕集苯的潜力。通过改变金属中心的大小但保持相同孔径上的苯环和桥联M-OH-M基团的修饰,我们在MFM-300(M)(M = Sc, VⅢ, Cr, Fe, Al, Ga, In)中进行了孔径尺寸的细微调整,结果得到了对苯/环己烷(体积比=1/1)分离的高选择性[最高可达MFM-300(Sc)的166]以及在1.2 mbar和298 K下对苯的高吸附性能,吸附量达到3.02 mmol g-1。通过原位同步辐射X射线粉末衍射(SXPD)和中子粉末衍射(NPD)、傅里叶变换红外显微光谱(FTIR)、固态核磁共振(ssNMR)和电子顺磁共振(EPR)光谱相结合,我们阐明了与苯和环己烷的选择性吸附机制以及观察到的偏好吸附苯而非环己烷的基础。我们报道了在UiO-66-CuⅡ中可见开放金属Cu(Ⅱ)位点与苯之间的可逆结合。MFM-300中孔径尺寸的变化对苯和环己烷分子的结合和排列产生了显著影响,从而实现它们的分离。本研究为设计新型MOF材料捕集微量苯和低碳净化环己烷在化学工业中提供了重要见解。
图文导读
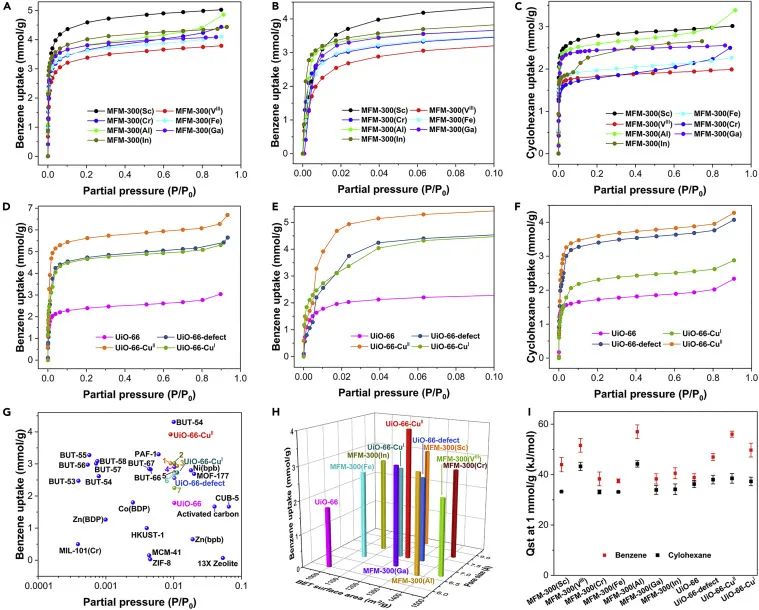
这些多孔材料的苯和环己烷单组分吸附等温线已记录下来,可在298-323 K的P/P0为0.9的范围内进行(图1A-1F)。所有等温线均显示出特征的Ⅰ型轮廓,苯的吸附量高于环己烷。然而,MFM-300(In)中环己烷吸附的等温线对应于Ⅳ型等温线,可能是由于主体材料存在一定程度的结构柔性造成的。这在先前负载p-二甲苯的MFM-300(In)的结构分析中已观察到。苯在这些MOF中的吸附表现出快速动力学特性,并在几分钟内达到平衡。尤其值得注意的是,在低压下苯的吸附量急剧增加,饱和度在P/P0约为0.02时达到,展示了这些MOF捕集痕量苯的潜力(图1B,1E)。这些MOF在298 K和1.2 mbar下展示出较高的苯吸附量,并与其他报道的苯吸附剂具有良好的比较性(图1G)。下面讨论的所有苯吸附量均指的是在298 K和1.2 mbar下收集的数据。具有最大孔径(8.1 Å)的MFM-300(Sc)在七种MFM-300材料中展示出最高的吸附量(3.02 mmol g-1)(2.28-3.02 mmol g-1)(图1H),吸附苯分子数与孔径呈部分相关关系。UiO-66-defect显示比UiO-66更高的吸附量(2.55 mmol g-1),这可以归因于前者存在缺陷位点以及稍高的孔隙度。重要的是,UiO-66-CuⅡ对苯的吸附量达到了3.92 mmol g-1的卓越水平,相较于UiO-66和UiO-66-defect分别提高了220%和154%。这个吸附量仅略低于同样条件下基准物质BUT-54(4.31 mmol g-1)的吸附量。由于其独特的电子性质、活性金属位点和高原子效率,单原子体系中包含原子分散的金属位点已成为催化领域的主要研究焦点。然而,在气体吸附应用方面,它们仍未得到充分研究。引入原子分散的Cu(Ⅱ)位点显著增强了UiO-66-CuⅡ中苯的吸附,为改善MOF在低压下对苯的吸附提供了新的途径。相反,通过还原UiO-66-CuⅡ得到的UiO-66-CuⅠ对苯的吸附量较低(2.74 mmol g-1),部分原因是Cu(Ⅰ)位点的Lewis酸性较弱。通过计算不同温度下测得的等温线,确定了吸附等温热(Qst)。高吸附负荷时,由于强烈的客体-客体相互作用,Qst值增加;低吸附负荷时,主体-客体相互作用占主导地位。MFM-300(Al)是个例外,其在高吸附负荷下Qst值减小,可能是由于窄孔直径限制了客体-客体相互作用。相反,MFM-300(Sc)在高吸附负荷下对苯的Qst值较高,这归因于较大的孔体积有利于苯分子的堆积。这些MOF对苯和环己烷的吸附是可逆的,加热至323K下动态真空可以完全去除吸附的客体分子。经过吸附-脱附循环后,这些MOF的结构和孔隙性能保持完整,具有较高的稳定性。
图1:单组分苯和环己烷气相吸附
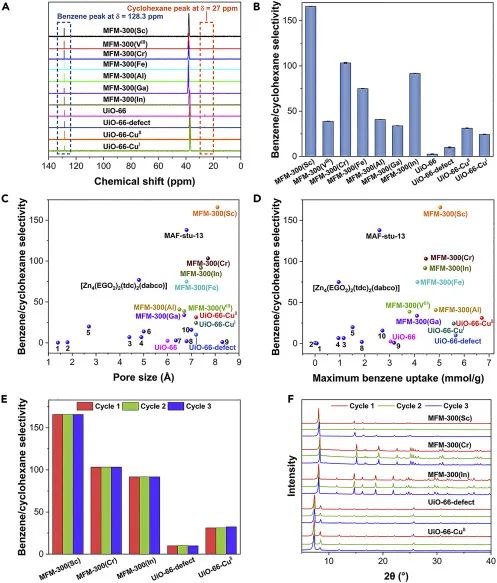
将活化后的MOF材料浸泡在苯和环己烷体积比为1/1的混合物中,保持24小时,温度为298K,进行苯/环己烷的分离。去除表面溶剂并消化吸附了客体的MOF后,使用1H NMR光谱测量了两种底物的整体吸附选择性(图2B)。所有这些MOF材料都显示出对苯优于环己烷的选择性吸附,苯/环己烷选择性大于34,并且观察到与孔径大小(6.5-8.1Å)有一般相关性(图2C)。值得注意的是,MFM-300(Sc)创造了新的苯/环己烷选择性基准值为166,超过了MAF-stu-13(138)。此外,有趣的是,除了Cu(Ⅱ)位点对苯的增强吸附作用外,UiO-66-CuⅡ和UiO-66-CuⅠ的选择性显著高于UiO-66,分别为31和24,证明在这些条件下,Cu(Ⅱ)和Cu(Ⅰ)位点能够增强苯/环己烷的分离效果。总体而言,对于苯的选择性与总吸附量的分析表明,与迄今报道的最佳材料相比,这些MOF材料在性能上表现出色(图2D)。
图2:苯/环己烷液相分离性能评价
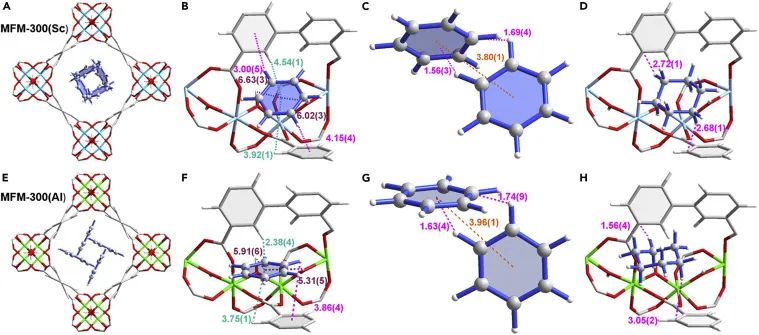
在所有七种MFM-300类似物中(图3A,3E),在通道内发现了苯的一个结合位点。每个苯分子以边-面T形或平行配置与框架的两个相邻芳香环结合,这由弱的-OH···π作用补充[-OH···苯中心=5.08(1)-6.63(3) Å](图3B,3F);通过NPD分析还确认了吸附的d6-苯与H-O桥羟基之间的-OH···π作用。这些等构质材料中宿主-客体结合的观察到的差异可以归因于孔内苯的不同堆积几何。MFM-300(Sc)的大孔直径使苯分子能够通过多个C-H···π相互作用[距离为3.00(5)-4.54(1) Å]与两个相邻的苯环发生强烈相互作用(图3B)。然而,在MFM-300(Al)的狭窄孔道中,苯分子被迫与一个苯环平行排列,并通过C-H···π [距离为3.75(1)-3.86(4) Å]相互作用进行结合(图3F)。这与苯/环己烷选择性与孔径之间的相关性一致。此外,客体苯分子之间的分子间相互作用通过垂直的T型构型观察到,其C-H···苯中心距离为1.56(3)-2.28(8) Å;具体来说,在MFM-300(Sc)和MFM-300(Al)中分别为1.56(3)和1.63(4) Å(图3C,3G)。重要的是,吸附的苯分子之间的分子间相互作用为低压下的高吸附提供了额外的协同驱动力。实际上,客体苯分子之间较短的C-H···π距离对应于低压下更高的吸附以及对苯的高选择性。有趣的是,吸附的苯分子形成了穿过框架通道的手性链。相反,环己烷与MFM-300的框架之间存在远程相互作用,其C-H···C距离范围为1.39(7)至3.05(2) Å。在MFM-300(Sc)中,结合的环己烷分子的最短C-H···C距离为2.68(1) Å,远大于MFM-300(Al)中的距离[1.56(4) Å],这表明环己烷在MFM-300(Sc)中的结合较弱,因此对苯与环己烷的选择性更高(图3D和3H)。
图3:MFM-300(Sc)和MFM-300(Al)中苯和环己烷的吸附位点示意图
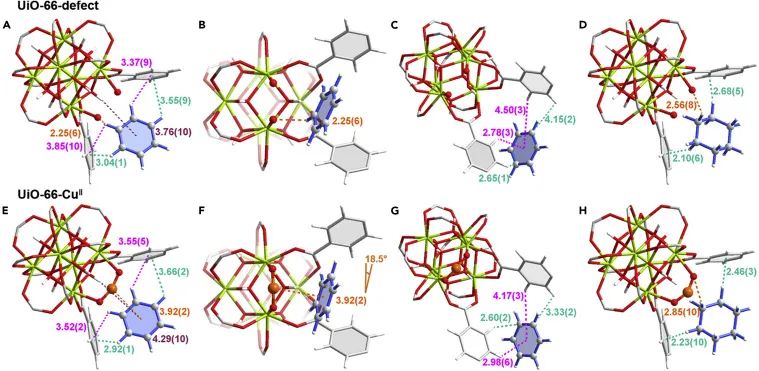
对于UiO-66系统,可以确定吸附苯分子的两个结合位点。位点I和位点II(在UiO-66-CuⅡ中每个{Zr6}的苯占据率分别为4.54和2.02)分别位于四面体空腔和八面体空腔中(图4A-4C、4E-4G、)。位点Ⅰ由配体的苯环和桥连羟基固定在原位,显示出C-H苯···π骨架相互作用[距离为3.37(9)-3.85(10) Å]和弱的-OH···π相互作用[O-H骨架···π苯=3.76(10)–4.29(10) Å]。此外,在UiO-66-defect中,吸附的苯分子与缺陷的-OH/-OH2位点有相互作用[C-H苯···Odefects=2.25(6) Å]。值得注意的是,在负载苯的UiO-66-CuⅡ和UiO-66-CuⅠ中观察到显著的CuⅡ···π相互作用[距离为3.92(2) Å]和CuⅠ···π相互作用[距离为3.89(2) Å],分别。这代表了对多孔MOF中Cu(Ⅱ)开放位点与苯分子结合的首次结构观察。位点Ⅱ主要通过C-H骨架···π苯相互作用来稳定[距离为2.43(1)–4.50(3) Å]。因此,相较于位点II,位点I通过更强的宿主-客体相互作用与骨架结合,这也与位点I的较高占有率是一致的。除了原始的UiO-66只显示四面体笼中的一个结合位点外,UiO-66系统中还观察到两个环己烷的结合位点(I'和II'),分别位于四面体空腔和八面体空腔中(图S23和S24)。所有吸附的环己烷分子都与骨架弱结合,其C-H环己烷···C骨架的距离为2.10(6)–4.35(4) Å,并伴随着在UiO-66-defect、UiO-66-CuⅡ和UiO-66-CuⅠ中的C-H环己烷···Odefects相互作用[距离为2.56(8)–2.92(11) Å],与其弱吸附性一致。因此,单原子Cu(Ⅱ)位点可以增强苯的结合能力,从而在低压下实现异常的吸附。
图4UiO-66缺陷和UiO-66-CuⅡ中苯和环己烷吸附位点的视图
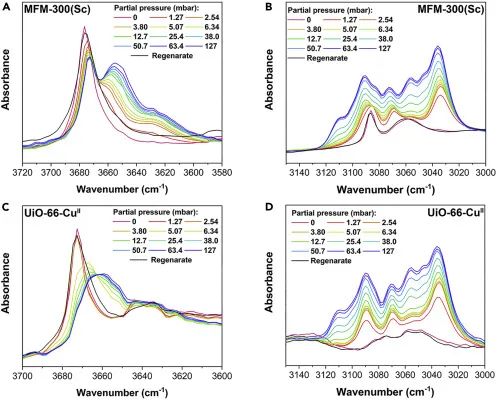
为了理解主体-客体结合动力学,对这些MOF在298K下以苯(0-127mbar)或环己烷(0-130mbar)的分压为函数进行原位傅立叶变换红外光谱测量(图5)。所有七种MFM-300材料在吸附苯时表现出类似的行为:观察到原始v(O-H)带(3,640-3,675 cm-1)的部分消耗,同时红移(Δ=2-4 cm-1)和新带的同步增长,新带通常比原始-OH带低约20 cm-1(图5A)。在353K和干燥N2流动条件下再生后,光谱恢复到原始状态,确认了–OH官能团与吸附苯分子之间可逆形成的–OH···π相互作用。然而,在这里观察到的v(O-H)带的变化小于报道的苯与硅胶上孤立羟基之间的强氢键的变化(Δ最高达140-170 cm-1)。这表明苯与框架的桥式羟基之间存在弱相互作用,与高度可逆的吸附行为一致。此外,在框架的C-H拉伸区域观察到C-H带(3,084-3,086cm-1)的蓝移(Δ=3 cm-1)以及苯的C-H带(3,090 cm-1)的显著增长,表明苯与框架的苯环之间存在相互作用(图5B)。这种变化在环己烷吸附时未被观察到,再次证实了环己烷与框架的弱结合。同样,在UiO-66-CuⅡ中,原始v(O-H)带的强度降低表明了框架中开放-OH基团的部分消耗,并同时伴随着–OH···π结合相互作用的可逆形成(图5C)。
图5原位MFM-300(Sc)和UiO-66-CuⅡ的FTIR光谱
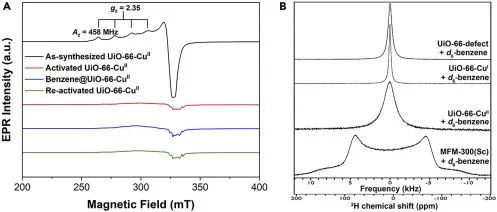
通过电子顺磁共振(EPR)光谱,研究了苯在UiO-66-CuⅡ中的结合情况(图6A)。原位合成的UiO-66-CuⅡ显示出具有dx2-y2或dxy基态的典型轴向Cu(Ⅱ)信号。激活样品导致配位水丧失和信号强度剧烈减小。这种行为在一些掺杂铜的沸石中也观察到过,并已经进行了描述,归因于Cu(Ⅱ)异常低配位几何构型。对于激活样品,吸附苯只引起EPR光谱微小变化,包括细微的展宽和垂直区域的微小变化。这与SXPD分析得出的Cu(Ⅱ)···苯距离为3.9 Å以及苯环与[O-Cu-O]平面之间的小二面角(18.5°)一致。关于苯在掺杂铜的沸石(MCM-41、K-L)中的吸附研究也显示出很小的连续波EPR光谱变化,电子自旋回波调制(ESEM)研究给出了Cu···H距离为4.1-4.2 Å,明显长于孤立金属芳烃配合物中的距离(例如,[Cr(0)(C6H6)2]中金属···芳烃中心的1.6 Å)。我们还可以排除在吸附过程中苯向Cu(Ⅱ)发生电子转移(形成自由基阳离子),这种现象对于脱水的掺杂铜黏土上的苯已经观察到了:在这里并未观察到这种物种。这个结果以及样品脱附后信号的进一步变化缺乏,确认了UiO-66-CuⅡ中苯吸附的高可逆性。
图6:EPR和2H NMR光谱
小结
综上所述,该研究报道了对一系列坚固的MOF材料进行苯吸附和苯/环己烷分离的全面研究。通过对孔道化学的精细调控和控制,它们在低压或存在环己烷和水的条件下显示出对苯高选择性吸附的巨大潜力,并具有优异的再生性和稳定性。通过晶体学分辨率揭示了关于这些MOF中苯结合的几个关键见解,并得到了多种光谱技术的支持。这些实验表明,在MFM-300系列中,MFM-300(Sc)由于客体苯分子与孔道表面的芳香环以及客体间相互作用之间的最佳主客体相互作用,而无需空金属位点,展现了最高的苯/环己烷分离选择性。相反,在UiO-66系统中,框架的苯环、缺陷位点以及最重要的单原子Cu(Ⅱ)中心促进了框架内苯的增强吸附。因此,具有原子级分散Cu(Ⅱ)位点的UiO-66-CuⅡ在捕获苯方面表现出卓越性能。MOF中孔径大小和孔内结构的合理设计为实现苯捕获和苯与环己烷吸附分离的高性能提供了有力途径。该研究将为今后设计和开发用于捕获微量挥发性有机物污染物和有机价值分离的新多孔材料提供指导。
参考文献:
Han, Y., et al. (2023) Control of the pore chemistry in metal-organic frameworks for efficient adsorption of benzene and separation of benzene/cyclohexane. Chem. doi.org/10.1016/j.chempr.2023.02.002